Barraquer apoya la cultura de la investigación entre los jóvenes
03/04/2025
10/11/2022
Las fases del desarrollo de un medicamento conforman varios procesos o etapas que culminan con la realización de los ensayos clínicos. Los ensayos, por su parte, también están divididos en diferentes fases que van desde la búsqueda de la dosis correcta, a través de unos pocos participantes, hasta la eficiencia del nuevo tratamiento en poblaciones de miles de personas. De forma paralela, se estudia la seguridad y eficacia del tratamiento, los efectos secundarios y la calidad de vida de los participantes en el estudio que administra el nuevo tratamiento.
Las diferentes etapas de un ensayo clínico son procesos secuenciales en los que se intenta demostrar que un nuevo fármaco es eficaz, efectivo, eficiente, seguro y que mejora la calidad de vida de los pacientes.
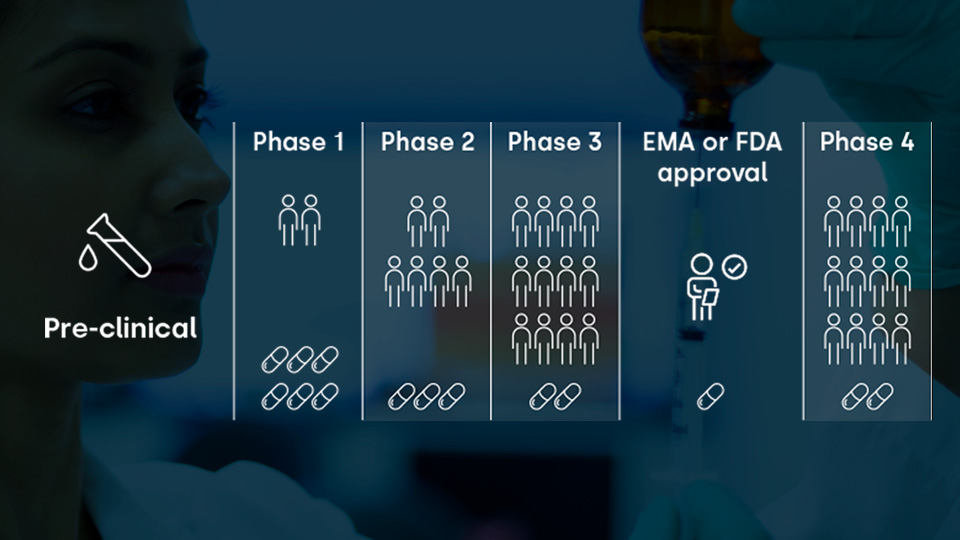
Fase preclínica
Antes de que el fármaco sea probado en seres humanos, para comprobar su eficacia y seguridad, se evalúa en animales. Si al final de este proceso, conocido como fase preclínica, se superan los requisitos necesarios, el fármaco pasaría a probarse en personas en un proceso que se denomina fase clínica, y que se divide asimismo en cuatro fases.
Fase clínica
Fase I. Evaluación de la seguridad
Permite entender cómo el fármaco actúa en el cuerpo, y cómo el cuerpo reacciona frente al fármaco (cómo se absorbe, se distribuye y se metaboliza). Esta primera etapa se caracteriza por administrar un nuevo tratamiento o una combinación nueva de fármacos, por primera vez a un humano sano. Al comienzo de la fase, se utilizan dosis bajas del fármaco, que se irán aumentando siempre y cuando el participante no esté expuesto a un riesgo. En algunos casos el paciente puede permanecer unos días en el hospital para un estrecho seguimiento.
Fase II. Evaluación de la eficacia
El objetivo principal es comprobar si el nuevo fármaco es eficaz en su nueva indicación. Se evalúan los efectos adversos a corto plazo y los riesgos de seguridad asociados al fármaco en investigación. Se administra el nuevo tratamiento por primera vez a un participante con la enfermedad a la que va dirigida el fármaco. Es decir, el fármaco tiene que demostrar que tiene un efecto terapéutico en la enfermedad para la cual ha sido diseñado. Pero también, en fármacos ya comercializados, puede buscar la eficacia en una nueva indicación. Se miden, además, los rangos de dosis, que van desde la dosis mínima que tiene un efecto, hasta la máxima dosis tolerada. En esta fase hay más participantes que en la anterior y la duración suele ser mayor.
Fase III. Confirmación de hallazgos en una población mayor de pacientes
El objetivo principal de esta tercera etapa es confirmar que el fármaco en investigación tiene un efecto terapéutico y que la seguridad de este es correcta. Si los resultados son positivos, se solicita la autorización del fármaco para uso clínico. En la fase III aumenta el número de participantes y la duración del ensayo, para así confirmar los datos recogidos en la fase II; también se realiza un balance de riesgo/beneficio más sólido que determinará si el fármaco puede comercializarse.
Fase IV. Revisión del tratamiento en práctica clínica
Son los estudios que se realizan una vez el fármaco está en el mercado y, por tanto, en una población mucho mayor. Están diseñados para evaluar la seguridad y eficacia del fármaco a largo plazo. El objetivo principal de esta fase es la de recopilar más datos en poblaciones más grandes y no homogéneas, ya sean sobre seguridad y eficacia, nuevas indicaciones o cuestiones económicas. Lo que permite, por ejemplo, saber si puede ser válido para otro tipo de enfermedad (nueva indicación), o si cuando se combina con otro fármaco se potencia el efecto terapéutico (sinergias). Pero también podremos ver más a fondo si tiene consecuencias graves cuando se padece una enfermedad diferente o se toma al mismo tiempo otra medicación (interacciones o contraindicaciones).
Victòria Hernández, Responsable del Área de Ensayos Clínicos